Výzkumníci z Massachusetts Institute of Technology (MIT) vyvinuli novou lipidovou nanočástici (LNP), která slibuje zlepšení účinnosti mRNA vakcín a potenciálně snížit náklady na dávku. Ve studiích na myších nový LNP úspěšně vyvolal imunitní odpověď ekvivalentní těm, kterých bylo dosaženo s existujícími materiály schválenými FDA, ale v přibližně 1/100 typické dávky.
Proč je to důležité?
mRNA vakcíny se ukázaly jako vysoce účinné proti nemocem, jako je COVID-19, ale jejich výroba může být nákladná. Snížení požadované dávky při zachování účinnosti nabízí několik výhod: snížené výrobní náklady, potenciálně méně vedlejších účinků a lepší dostupnost pro globální iniciativy v oblasti zdraví.
Věda v pozadí inovací
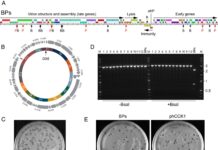
Současné mRNA vakcíny jsou uzavřeny uvnitř LNP – drobných, mastných kuliček – aby chránily křehkou mRNA před degradací a usnadňovaly její vstup do buněk. Tyto částice se typicky skládají z pěti klíčových složek: ionizovatelný lipid (důležitý pro účinnost vakcíny), cholesterol, doplňkový fosfolipid, polyethylenglykol lipid a mRNA. Tým MIT se zaměřil na optimalizaci ionizovatelného lipidu, aby se zlepšila efektivita dodání.
Nový design
Výzkumníci vyvinuli a prozkoumali knihovnu nových ionizovatelných lipidů, včetně cyklických struktur pro zlepšení dodávání mRNA a esterových skupin pro zlepšení biologické rozložitelnosti. Prostřednictvím několika kol screeningu na myších identifikovali LNP s nejlepším výkonem, nazvaný AMG1541. Jednou z klíčových výhod AMG1541 je jeho vynikající schopnost překonat „endosomový výstup“, kritický krok, ve kterém LNP musí opustit buněčné kompartmenty zvané endozomy, aby dodaly svou mRNA. Nové částice také rychleji degradují po dodání jejich obsahu, což potenciálně minimalizuje vedlejší účinky.
Slibné výsledky ve studiích vakcín proti chřipce
K vyhodnocení skutečného potenciálu vědci použili AMG1541 LNP k dodání vakcíny proti chřipce na bázi mRNA u myší. Ve srovnání s vakcínou proti chřipce používající SM-102, lipid již schválený pro vakcíny COVID-19 (používané společností Moderna), nová LNP konzistentně generovala stejnou protilátkovou odpověď pouze s 1/100 dávkou.
Posílená imunitní odpověď a potenciál pro rychlý vývoj vakcíny
Další výzkum ukázal, že nové LNP byly efektivnější při doručování svého nákladu do buněk prezentujících antigen – důležitých imunitních buněk, které zobrazují cizí antigeny, aby aktivovaly jiné imunitní buňky (jako jsou B a T buňky). Navíc mají tendenci se hromadit v lymfatických uzlinách, čímž se zvyšuje interakce s imunitním systémem. To by mohlo vést k přesnějšímu a rychlejšímu vývoji vakcín proti sezónní chřipce, což je významná výhoda oproti tradičním harmonogramům výroby vakcín, které často vyžadují zahájení výroby téměř rok předem.
Širší aplikace
Vědci se domnívají, že tyto nanočástice by mohly být přizpůsobeny pro vakcíny zaměřené na jiné infekční nemoci, včetně COVID-19, HIV a dalších. “Zjistili jsme, že fungují mnohem lépe než cokoli, co bylo dříve hlášeno. Proto si myslíme, že u všech intramuskulárních vakcín lze naše platformy LNP použít k vývoji vakcín proti řadě nemocí,” řekl Gupta, výzkumník z Kochova institutu.
Vývoj těchto nových LNP představuje důležitý krok směrem k dostupnějším a dostupnějším mRNA vakcínám, které dláždí cestu pro lepší globální zdravotní výsledky.